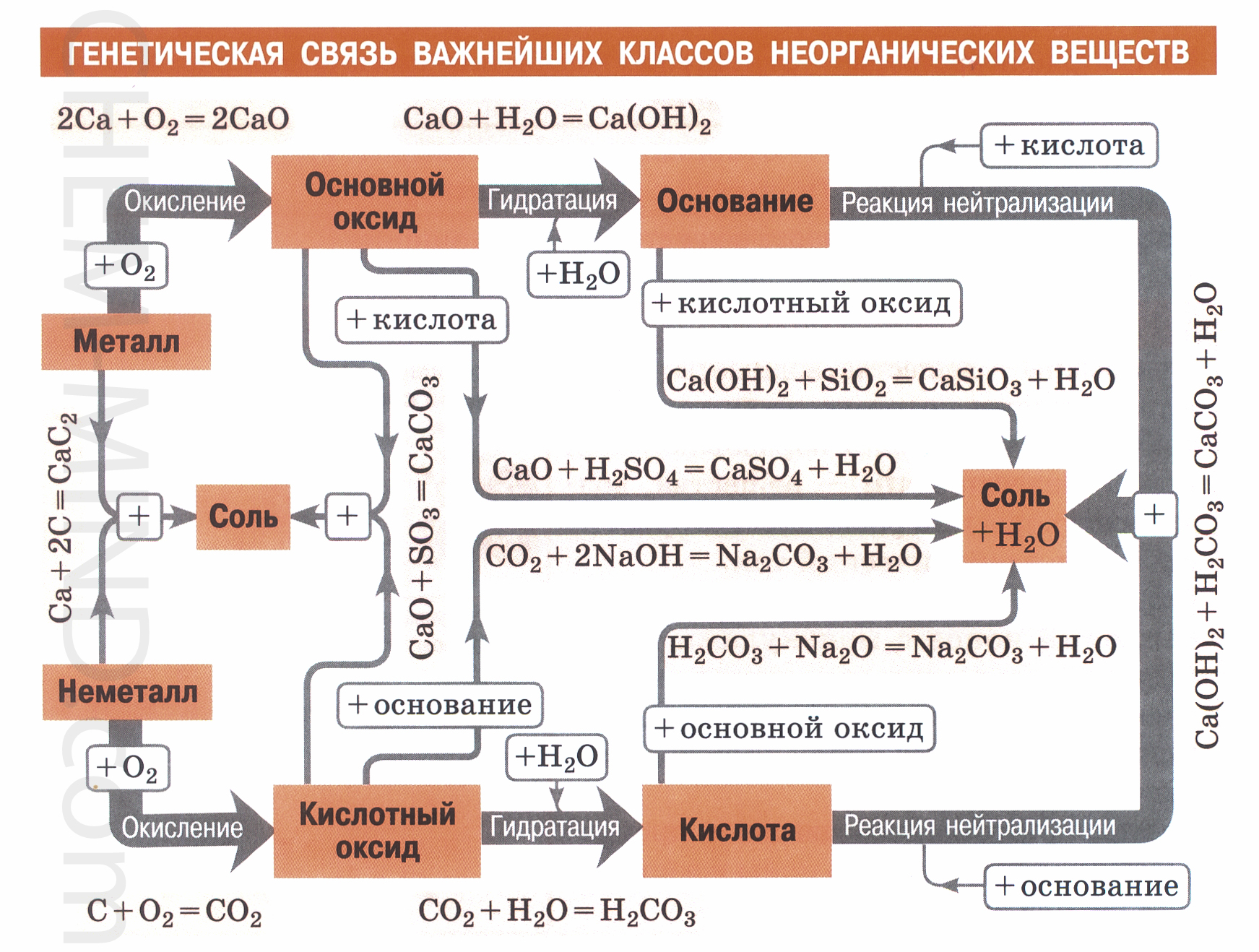
Kết nối di truyền giữa các lớp của các chất vô cơ. Kết nối di truyền của kim loại, phi kim loại và các hợp chất của chúng
Truyền thông di truyền. - Đây là mối quan hệ giữa các chất liên quan đến các lớp khác nhau.
Các dấu hiệu chính của loạt di truyền:
1. Tất cả các chất của một hàng phải được hình thành bởi một yếu tố hóa học.
2. Các chất được hình thành bởi cùng một yếu tố phải thuộc nhiều loại hóa chất khác nhau.
3. Các chất tạo thành một dải di truyền của một yếu tố phải được kết nối với nhau.
Theo cách này, Di truyền.chúng được gọi là một số chất đại diện cho các loại hợp chất vô cơ khác nhau là các hợp chất của cùng một yếu tố hóa học, được liên kết với các cuộc phiêu lưu lẫn nhau và phản ánh tính tổng quát của nguồn gốc của các chất này.
Đối với kim loại, ba hàng chất liên quan đến gen bị cô lập, đối với phi kim loại - một hàng.
1. Hàng kim loại di truyền có hydroxit là căn cứ (kiềm):
kim loại→ Oxit chính→ cơ sở (kiềm)→ Muối.
Ví dụ, loạt canxi di truyền:
CA → Cao → CA (OH) 2 → Cacl 2
2. Hàng kim loại di truyền tạo thành hydroxit amphoteric:
muối
kim loại→ oxit amphoteric→ (Muối)→ amphoteric hydroxide.
Ví dụ: ZNCL 2
Zn → zno → znso 4 → zn (oh) 2
(H 2 ZnO 2) ↓
Na 2 zno 2
Oxit kẽm với nước không tương tác, do đó, nó lần đầu tiên được lấy từ nó, và sau đó kẽm hydroxit. Cũng đến nếu kim loại tương ứng với một cơ sở không hòa tan.
3. Dòng di truyền không kim loại (không kim loại chỉ được hình thành các oxit axit):
phi kim loại.→ Oxit axit.→ axit→ Muối
Ví dụ, dải di truyền của phốt pho:
P → P 2 O 5 → H 3 PO 4 → K 3 PO 4
Việc chuyển từ một chất này sang chất khác được thực hiện bằng phản ứng hóa học.
Chủ đề: Kết nối di truyền giữa kim loại và phi kim loại và hợp chất của chúng. lớp 9.
Mục tiêu: Giáo dục: củng cố các khái niệm về "loạt di truyền", "kết nối di truyền"; Dạy loạt các yếu tố di truyền (kim loại và phi kim loại), để vẽ các phương trình phản ứng tương ứng với loạt di truyền; Kiểm tra kiến \u200b\u200bthức về các tính chất hóa học của oxit, axit, muối, cơ sở; phát triển: phát triển khả năng phân tích, so sánh, tóm tắt và rút ra kết luận, để rút ra các phương trình phản ứng hóa học; Giáo dục: Thúc đẩy sự hình thành của thế giới quan khoa học.
Đảm bảo các lớp: Bảng "Hệ thống định kỳ", "Bảng hòa tan", "Dòng hoạt động kim loại", hướng dẫn cho sinh viên, nhiệm vụ để thử nghiệm kiến \u200b\u200bthức.
Động thái làm việc: 1) org. chốc lát
2) Kiểm tra D / S
3) Nghiên cứu một tài liệu mới
4) Hợp nhất
5) D / S
1) org. chốc lát. Lời chào.
2) Kiểm tra D / S.

Các kết nối di truyền là các kết nối giữa các lớp khác nhau dựa trên các vọt đối của chúng.
Biết các lớp các chất vô cơ, chúng ta có thể tạo ra các hàng di truyền kim loại và không kim loại. Cơ sở của các hàng này là cùng một yếu tố.
Trong số các kim loại bạn có thể phân bổ hai loại hàng:
1 . Hàng di truyền trong đó nó được chọn như một cơ sở. Sê-ri này có thể được biểu diễn bằng các biến đổi sau:
kim loại → Ôxít chính → Schemochi → Muối
Ví dụ: k → k 2 O → koh → kcl
2 . Dòng di truyền, nơi một cơ sở không hòa tan hoạt động như một cơ sở, sau đó một số có thể được thể hiện bằng một chuỗi các biến đổi:
kim loại → Ôxít chính → Muối → Cơ sở không hòa tan →
→Ôxít chính → Kim loại
Ví dụ: cu → cuo → cucl 2 → Cu (OH) 2 → cuo → cu
1 . Một loạt di truyền của phi kim loại, nơi axit hòa tan hoạt động như một liên kết của một số. Chuỗi biến đổi có thể được biểu diễn như sau:
phi kim → axit oxit → axit hòa tan → muối
Ví dụ: p → p 2 Vả lại 5 → H. 3 Thuộc về Po. 4 → Na. 3 Thuộc về Po. 4
2 . Dòng di truyền của phi kim loại, trong đó axit không hòa tan hoạt động như một liên kết của một số:
phi kim loại → oxit axit → muối → axit →
→oxit axit → phi kim
Ví dụ,Si.→ Sio. 2 → Na. 2 Sio. 3 → Hòx 2 Sio. 3 → Sio. 2 → Si.

Cuộc trò chuyện giữa các câu hỏi:
Mối quan hệ di truyền là gì? Các kết nối di truyền là kết nối giữa các lớp khác nhau dựa trên các vọt đối của chúng. Bộ di truyền là gì?
Dòng di truyền - một số chất - đại diện của các lớp khác nhau là các hợp chất của một nguyên tố hóa học liên quan đến chuyển đổi lẫn nhau và phản xạ của các chất này. Cơ sở của các hàng này là cùng một yếu tố.
Những loại loạt di truyền được thực hiện để phân bổ? Trong số các kim loại, hai loại hàng có thể được phân biệt:
a) một hàng di truyền trong đó nó đứng như một cơ sở. Sê-ri này có thể được biểu diễn bằng các biến đổi sau:
kim loại → Ôxít chính → Schemochi → Muối
ví dụ, một hàng di truyền kali k → k 2 O → koh → kcl
b) Một loạt di truyền, trong đó một cơ sở không hòa tan hoạt động như một cơ sở, sau đó một số có thể được thể hiện bằng một chuỗi các biến đổi:
kim loại → Ôxít chính → Muối → Cơ sở không đẹp → Ôxít chính → Kim loại
ví dụ: cu → cuo → cucl 2 → Cu (OH) 2 → cuo → cu
Trong số các phi kim loại cũng có thể được phân biệt bởi hai loại cấp bậc:
a) Một loạt các phi kim loại di truyền, nơi axit tan hoạt động như một liên kết của một số. Chuỗi biến đổi có thể được biểu diễn như sau: phi kim loại → oxit axit → axit hòa tan → muối.
Ví dụ: P → P 2 Vả lại 5 → H. 3 Thuộc về Po. 4 → Na. 3 Thuộc về Po. 4
b) một chuỗi di truyền không kim loại, trong đó axit không hòa tan hoạt động như một loạt các hàng: không kim loại → oxit axit → muối → axit → oxit axit → phi kim loại
Ví dụ: si → sio 2 → Na. 2 Sio. 3 → H. 2 Sio. 3 → SIO. 2 → SI.
Thực hiện các nhiệm vụ theo các tùy chọn:
1. Chọn trong phiên bản công thức oxides của bạn, giải thích sự lựa chọn của bạn, dựa trên kiến \u200b\u200bthức về các dấu hiệu của lớp hợp chất này. Hãy gọi tên của chúng.
2. Trong cột của các công thức tùy chọn của bạn, tìm các công thức axit và giải thích sự lựa chọn của bạn dựa trên phân tích thành phần của các hợp chất này.
3. Xác định hóa trị dư lượng axit trong thành phần của axit.
4. Chọn Công thức trục và đặt tên cho chúng.
5. Tạo công thức muối có thể được hình thành bởi magiê và axit của tùy chọn của bạn. Viết chúng xuống, tên.
6. Trong cột của các công thức của tùy chọn của bạn, tìm các công thức của căn cứ và giải thích sự lựa chọn của bạn dựa trên phân tích thành phần của các hợp chất này.
7. Trong hiện thân của bạn, chọn công thức các chất mà dung dịch acid orthophosphoric (muối, lưu huỳnh) có thể phản ứng. Thực hiện các phương trình thích hợp của phản ứng.
9. Trong số các công thức cho tùy chọn của nó, chọn công thức các chất có thể tương tác với nhau. Thực hiện các phương trình thích hợp của phản ứng.
10. Tạo một chuỗi liên kết di truyền của các hợp chất vô cơ, sẽ bao gồm một chất, công thức được đưa ra trong phiên bản của bạn tại số một.
lựa chọn 1
Lựa chọn 2.
Cao.
HNO. 3
FE (OH) 3
N. 2 Vả lại
Zn (Không. 3 ) 2
Cr (oh) 3
Hòx 2 VÌ THẾ. 3
Hòx 2 S.
Pbo.
Lioh.
Ag. 3 Thuộc về Po. 4
P. 2 Vả lại 5
Naoh.
ZnO.
Công ty TNHH 2
BACL. 2
HCl.
Hòx 2 Công ty TNHH 3
Hòx 2 VÌ THẾ. 4
Cuso. 4
Từ các chất này, tạo một loạt di truyền bằng cách sử dụng tất cả các công thức. Viết các phương trình phản ứng mà bạn có thể thực hiện chuỗi biến đổi này:
Tôi chọn: znso 4, Zn, ZnO, Zn, Zn (OH) 2 : II. Lựa chọn:Na. 2 VÌ THẾ. 4, Naoh., Na., Na. 2 Vả lại 2 , Na. 2 Vả lại
4) hợp nhất1.Al.→ Al. 2 Vả lại 3 → Alcl. 3 → Al.( Oh.) 3 → Al. 2 Vả lại 3
2. P.→ P. 2 Vả lại 5 → Hòx 3 Thuộc về Po. 4 → Na. 3 Thuộc về Po. 4 → CA. 3 ( Thuộc về Po. 4 ) 2
3. Zn → ZNCL 2 → zn (oh) 2 → ZnO → Zn (không 3 ) 2
4.Cu → CuO → CUCL 2 → Cu (OH) 2 → cuo → cu
5.N. 2 Vả lại 5 → HNO. 3 → Fe (không 3 ) 2 → Fe (oh) 2 → fes → feso 4
5) bài tập về nhà: Tạo một sơ đồ chuyển đổi dần dần từ canxi đến canxi cacbonat và chuẩn bị một thông điệp về việc sử dụng bất kỳ muối nào trong y học (sử dụng thêm tài liệu).
Thế giới vật chất mà chúng ta sống và phần nhỏ của chúng ta, và đồng thời là vô cùng đa dạng. Sự thống nhất và sự đa dạng của các hóa chất của thế giới này được phát âm nhất trong kết nối di truyền của các chất, được phản ánh trong cái gọi là thứ hạng di truyền. Chúng tôi làm nổi bật các dấu hiệu đặc trưng nhất của các hàng như vậy.
1. Tất cả các chất của loạt phim này phải được hình thành bởi một yếu tố hóa học. Ví dụ: một loạt đã ghi bằng các công thức sau:
2. Các chất được hình thành bởi cùng một yếu tố phải thuộc về các lớp khác nhau, tức là để phản ánh các hình thức tồn tại khác nhau của nó.
3. Các chất tạo thành một chuỗi di truyền của một yếu tố phải được liên kết với hỗ trợ lẫn nhau. Tính năng này có thể phân biệt chuỗi di truyền hoàn chỉnh và không đầy đủ.
Ví dụ, loạt di truyền brom được đề cập ở trên sẽ không đầy đủ, chưa hoàn thành. Và đây là loạt sau:
bạn đã có thể được xem như một sự hoàn chỉnh: anh ấy bắt đầu với một chất brom đơn giản và nó đã kết thúc.
Tóm tắt những điều trên, bạn có thể đưa ra định nghĩa sau đây của loạt di truyền.
Loạt di truyền. - Đây là một số chất - đại diện của các lớp khác nhau là các hợp chất của một nguyên tố hóa học liên quan đến lẫn nhau và phản ánh tính tổng quát của nguồn gốc của các chất này hoặc Genesis của chúng.
Truyền thông di truyền. - Khái niệm chung hơn chuỗi di truyền, cũng là một biểu hiện sáng sủa, nhưng riêng tư của kết nối này, được thực hiện với bất kỳ biến đổi nào về các chất. Sau đó, rõ ràng, loạt các chất giảm đầu tiên cũng phù hợp với định nghĩa này.
Có ba loại loạt di truyền:
Người giàu nhất trong một hàng kim loại, biểu hiện các mức độ oxy hóa khác nhau. Ví dụ, hãy xem xét hàng gen gen với độ oxy hóa +2 và +3:

Nhớ lại rằng để oxy hóa sắt trong Iron clorua (II), cần phải đi oxy hóa yếu hơn là có được Iron clorua (III):

Tương tự như một hàng kim loại giàu hơn trong các kết nối nhiều hơn một số loại kim loại có độ oxy hóa khác nhau, ví dụ, một loạt lưu huỳnh di truyền với độ oxy hóa +4 và +6:

Khó khăn chỉ có thể gây ra sự chuyển đổi cuối cùng. Quy tắc tính năng: Để có được một chất đơn giản từ kết nối phần tử bị oxy hóa, bạn cần thực hiện kết nối được khôi phục nhiều nhất cho mục đích này, ví dụ, một hợp chất hydro không có dơi. Trong trường hợp của chúng ta:
Theo phản ứng này, lưu huỳnh được hình thành trong tự nhiên từ khí đốt.
Tương tự như clo:
3. Hàng kim loại di truyền, tương ứng với oxit amphoteric và hydroxit,rất giàu kết nối, vì họ tập thể dục tùy thuộc vào các điều kiện có tính axit, sau đó các thuộc tính cơ bản.
Ví dụ, hãy xem xét hàng di truyền của kẽm:

Mối quan hệ di truyền giữa các lớp vô cơ
Các phản ứng giữa các đại diện của loạt di truyền khác nhau là đặc trưng. Các chất từ \u200b\u200bmột loạt di truyền, như một quy luật, không tham gia vào tương tác.
Ví dụ:
1. Kim loại + phi kim \u003d muối
Hg + s \u003d hgs
2AL + 3I 2 \u003d 2ALI 3
2. Ôxít chính + axit oxit \u003d muối
Li 2 o + co 2 \u003d li 2 co 3
Cao + SIO 2 \u003d Casio 3
3. BASE + ACID \u003d Muối
CU (OH) 2 + 2HCL \u003d CUCL 2 + 2H 2 O
FECL 3 + 3HNO 3 \u003d FE (NO 3) 3 + 3HCL
axit muối muối muối
4. Kim loại - Ôxít chính
2CA + O 2 \u003d 2CAO
4li + o 2 \u003d 2li 2 o
5. Không kim loại - oxit axit
S + O 2 \u003d Vậy 2
4AS + 5O 2 \u003d 2AS 2 O 5
6. Ôxít chính - Cơ sở
Bao + h 2 o \u003d ba (oh) 2
Li 2 o + h 2 o \u003d 2lioh
7. Oxit axit - axit
P 2 O 5 + 3H 2 O \u003d 2H 3 PO 4
Vì vậy, 3 + H 2 O \u003d H 2 So 4
Hướng dẫn cho sinh viên về tỷ lệ tương ứng "hóa học chung cho lớp 12" 1. Danh mục sinh viên: Tài liệu của bài thuyết trình này được cung cấp một người học để nghiên cứu độc lập các chủ đề "Các chất và tài sản của họ", từ quá trình phân loại chung của lớp 12 . 2. Nội dung khóa học: Bao gồm 5 bài thuyết trình cho những người. Mỗi chủ đề giáo dục chứa một cấu trúc rõ ràng của tài liệu giáo dục về một chủ đề cụ thể, kiểm tra slide cuối cùng - các nhiệm vụ tự kiểm soát. 3. Ít thời gian trong khóa học này: Từ một tuần đến hai tháng (nó được xác định riêng lẻ). 4. Kiểm soát kiến \u200b\u200bthức: Học sinh cung cấp một báo cáo về hiệu suất của các tác vụ thử nghiệm - một tờ có tùy chọn cho các tác vụ, cho biết chủ đề. 5. Đánh giá kết quả: "3" - 50% các nhiệm vụ được đáp ứng, "4" - 75%, "5" Tác vụ. 6. Kết quả học tập: chủ đề của chủ đề được nghiên cứu.


Phương trình phản ứng: 1. 2CU + O 2 2CUO Copper Oxide (II) 2. CuO + 2 HCL CUCL 2 + H 2 O Copper Clorua 3. Cucl Naoh Cu (OH) Na CL Đồng Hydroxide (II) 4. Cu (OH) 2 + H 2 so 4 cuso 4 + 2n 2 o đồng sulfate (II)



Chuỗi gen của các hợp chất hữu cơ. Nếu cơ sở của loạt hóa học vô cơ là một chất được hình thành bởi một nguyên tố hóa học, cơ sở của loạt di truyền trong hóa học hữu cơ là một chất có cùng số nguyên tử carbon trong phân tử.

Đề án phản ứng: Mỗi chữ số trên mũi tên tương ứng với một phương trình phản ứng cụ thể: ethanol ethanol ethan ethane ethane chlorhetan edic acetic (ethan) axit

Các phương trình phản ứng: 1. C 2 H 5 CL + H 2 O C 2 H 5 OH + HCL 2. C 2 H 5 OH + O CH 3 CH O + H 2 O 3. CH 3 CH O + H 2 C 2 5 OH 4. C 2 H 5 OH + HCL C 2 H 5 CL + H 2 O 5. C 2 H 5 CL C 2 H 4 + HCL 6. C 2 H 4 C 2 H 2 + H 2 7. C 2 H 2 + H 2 O CH 3 CH O 8. CH 3 CH O + AG 2 O CH 3 SOOH + AG


